
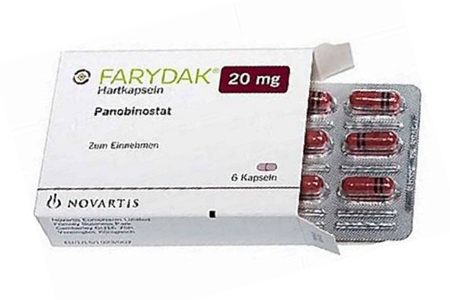
帕比司他由诺华(Novartis Pharmaceuticals Corporation)研发并推广,商品名FARYDAK,最早于2015年在美国获批上市。 帕比司他为多发性骨髓瘤患者提供了新的治疗选择,特别是在既往标准方案失败后,能够延长无进展生存期。因其独特的抗肿瘤机制及加速获批的临床需求,目前正被纳入更多临床实践和研究中。
本说明书旨在为临床医师和药学人员提供帕比司他的适应症、用法用量、特殊人群用药等系统化、专业化的信息,为安全、规范地应用该药提供指导。
帕比司他
既往接受过至少两种治疗方案(包含硼替佐米和一种免疫调节剂)的复发/难治性多发性骨髓瘤患者。
胶囊:10mg(浅绿色,6粒/板)、15mg(橙色,6粒/板)、20mg(红色,6粒/板)。
【孕妇】禁用,实验动物致畸;
【哺乳期女性】未知乳汁排泄情况,建议停药或停止哺乳;
【生殖潜力人群】女性用药期间及停药后1 月避孕;男性用药期间及停药后3 月避孕;
【儿童】安全性与有效性未建立;
【老年人】65岁以上患者骨髓抑制及胃肠、心脏毒性风险增高,应加强监测;
【肾功能损害】轻至重度肾损害(CrCl<30 mL/min)对药物暴露无显著影响,ESRD/透析者未评价;
【肝功能损害】轻度起始15mg,中度10mg,重度禁用。
经验有限,可能加剧骨髓抑制及胃肠道毒性(如腹泻、恶心、呕吐等);应监测心电及电解质并予纠正,必要时输血或血小板支持;透析清除性未知。
24个月
20℃-25℃贮存(允许15℃~30℃),避光,原包装内保存;胶囊不可打开、碾碎或咀嚼,避免粉末接触皮肤/黏膜,如接触应立即用水清洗
帕比司他主要经CYP3A(约40%)、CYP2D6、CYP2C19及UGT途径代谢。
免责声明:本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
参考资料: